Gesundheit, Impfaufklärung
Impfstoffe - Über 200 Ärzte und Apotheker fordern Verbesserung der Zulassungsverfahren
Ärzte und Apotheker fordern in einer Aktion der DAGIA (Deutsche Arbeitsgemeinschaft für unabhängige Impfaufklärung) die Einhaltung von Mindeststandards bei Zulassungsstudien von Impfstoffen. Über 200 Mediziner (Stand Dez. 2015) haben ein 10 Punkte Programm unterzeichnet mit dem Ziel, eine Fachdiskussion anzuregen.
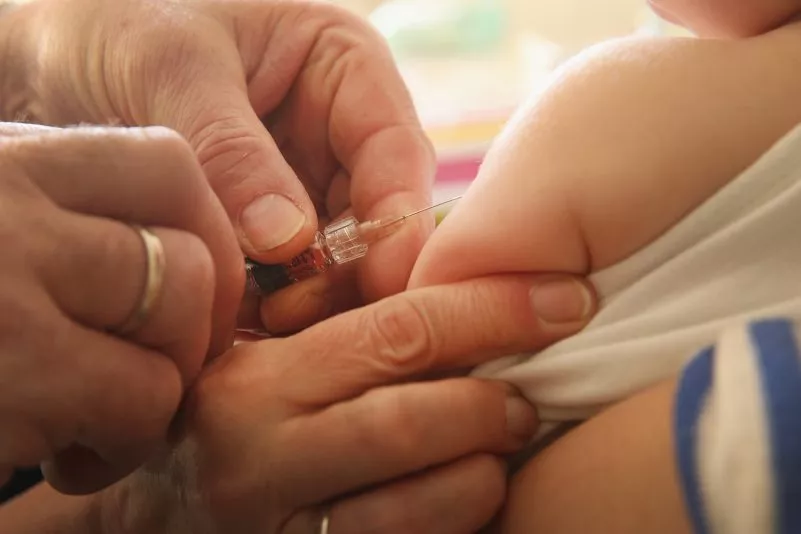
Foto: Sean Gallup/Getty Images
Aus der Sicht der DAGIA (Deutsche Arbeitsgemeinschaft für unabhängige Impfaufklärung) erfüllt die derzeitige Zulassungspraxis nicht die Kriterien für einen evidenzbasierten Einsatz von Impfstoffen. Laut des Aktionskreises gibt es in Fachkreisen bisher keine echte Diskussion über Mindestanforderungen und so hat sie sich als unabhängige Institution zum Ziel gesetzt, eine entsprechende Fachdiskussion anzuregen. Ärzte, die die aufgeführten 10 Forderungen für sinnvoll halten, können dies durch die Eintragung in eine Unterstützerliste dokumentieren. Das Ziel der DAGIA ist, diesen Forderungen durch eine möglichst große Anzahl von Unterstützern ein gesundheitspolitisches Gewicht zu verleihen. Hier nun die Aktionsschrift, wie sie Ärzten und Mitgliedern anderer medizinischer Berufe angeboten wird:
Mindest-Anforderungen an evidenzbasierte Zulassungsstudien
Impfungen gelten als eine der größten Errungenschaften der modernen Medizin. Sie stellen jedoch rechtlich gesehen Körperverletzungen dar, die darum der mündigen Einwilligung bedürfen. Zudem handelt es sich um nicht unmittelbar notwendige medizinische Eingriffe an Gesunden. Deshalb sind besonders hohe Anforderungen an ihre Zulassung zu stellen. Ziel dieser Anforderungen muss sein, eine deutliche und statistisch zuverlässige Aussage bezüglich eines gesundheitlichen Vorteils von Geimpften gegenüber Ungeimpften treffen zu können. Wir fordern deshalb die Einhaltung eines Mindeststandards:
1. Randomisierter, placebokontrollierter und mehrfach verblindeter Vergleich zwischen Geimpften und Ungeimpften (bzw. Placebo-Geimpften)
Solche Studien werden in der Regel nicht durchgeführt, denn es ist angeblich unethisch, Probanden bewusst einen Wirkstoff vorzuenthalten. Bei einem noch ungetesteten Impfstoff kann man jedoch nicht von einer Wirksamkeit ausgehen! Interessanterweise sind vergleichende Blindstudien selbst im Veterinärbereich nicht üblich, obwohl das Ethik-Argument dort nicht greift. Außerdem werden in den letzten Jahren ständig „unethische“ Ausnahmen gemacht (siehe z. B. Gardasil, Cervarix, Zostavac, Rotarix). Das Ethik-Argument macht keinen Sinn!
2. Zwingende Eintragung in ein öffentliches Studienregister
Viele Hersteller neigen dazu, Studien mit unerwünschten Ergebnissen gar nicht erst zu veröffentlichen. Das Fehlen einer Studienregister-Verpflichtung wird deshalb seit Jahrzehnten von Fachkreisen und med. Fachzeitschriften bemängelt.
3. Keine Schein-Placebos!
Schein-Placebos, die Impfstoffbestandteile (z. B. Aluminiumhydroxid) enthalten, führen zu gravierenden Verzerrungen der Studienergebnisse!
4. Ausreichende Größe und Laufzeit
Die meisten Studien sind zu klein und laufen nicht lange genug, um zuverlässige Daten zu Wirksamkeit und Sicherheit liefern zu können.
5. Transparenz des Studiendesigns
Das Studiendesign mitsamt allen relevanten (anonymisierten) Daten, die für die Beurteilung einer Studie wichtig sind, unterliegt bisher grundsätzlich der Geheimhaltung durch Behörden und Hersteller. Eine Gegenprüfung durch die Fachwelt wird dadurch unmöglich gemacht.
6. Erfassung aller (!) verfügbarer Gesundheitsparameter
Durch das gezielte Auswählen bestimmter klinischer Endpunkte kann das Ergebnis einer Studie leicht in sein Gegenteil verkehrt werden.
7. Unabhängiger Ansprechpartner für Probanden
Denn manche Studienärzte tendieren erfahrungsgemäß dazu, mögliche Impfkomplikationen gegenüber Probanden zu bagatellisieren.
8. Finanzielle und organisatorische Unabhängigkeit vom Hersteller
Zahlreiche Publikationen belegen, dass herstellerfinanzierte Studien tendenziös sind. Hierfür muss eine Lösung gefunden werden.
9. Völlig ungeimpfte Kontrollgruppe
Um zu überprüfen, ob durch die speziellen Bedingungen der Studie ein falsches Bild der Epidemiologie erzeugt wird.
10. Nachmarktstudien
Nachmarktstudien sind wichtig, um das Ergebnis der Zulassungsstudien zu ergänzen – oder zu korrigieren. Sie sind bisher nicht verpflichtend, ja das PEI hat als deutsche Zulassungsbehörde noch nicht einmal einen Überblick über die verfügbaren Nachmarktstudien!
Weitere Informationen zu dieser Aktion unter www.dagia.org
(mh)
Kommentare
Noch keine Kommentare – schreiben Sie den ersten Kommentar zu diesem Artikel.
0
Kommentare
Noch keine Kommentare – schreiben Sie den ersten Kommentar zu diesem Artikel.





